NỘI DUNG WEB
» 422 Bài giảng chẩn đoán hình ảnh
» X-quang / Siêu âm / CT Scan / MRI
» 25.000 Hình ảnh case lâm sàng
ĐỐI TƯỢNG
» Kỹ thuật viên CĐHA
» Sinh viên Y đa khoa
» Bác sĩ khối lâm sàng
» Bác sĩ chuyên khoa CĐHA
Nội dung Bài giảng & Case lâm sàng thường xuyên được cập nhật !
Đăng nhập Tài khoản để xem Nội dung Bài giảng & Case lâm sàng !!!
– Khoang sau phúc mạc nằm phía trước mạc ngang và phía sau phúc mạc thành. * Giải phẫu các khoang: – Giới hạn: – Giới hạn: – Giới hạn: mạc quanh thận – Giới hạn: mạc quanh thận. – Hợp bởi nhiều lớp của mạc treo phôi thai => ngăn ảo giữa các khoang sau phúc mạc. – Mặt phẳng sau mạc treo (RMP) – Mặt phẳng sau thận (RRP) – Mặt phẳng cạnh nón (LCP): giữa các lá của cân nón bên. Các mặt phẳng sau mạc treo, mặt phẳng sau thận và mặt phẳng cạnh nón kết hợp tại một điểm. – Mặt phẳng gian cân phối hợp (Combined interfascial plane – CIP) hợp nhất giữa cân Gerota và cân Zuckerkandl chạy xuống tận tiểu khung. – Cầu nối quanh thận (Perinephric bridging septa) hoặc vách ngăn Kunin bao gồm rất nhiều lá xơ mỏng đi qua mỡ quanh thận, treo thận trong khoang quanh thận. Chúng có thể như một rào cản cho sự lây lan của mủ, máu, nước tiểu trong khoang quanh thận. – Khoang mỡ trước phúc mạc (properitoneal fat) là 1 khoang nằm trước phúc mạc, chứa tổ chức mỡ. – Xác định khối u thuộc khoang sau phúc mạc: + Đè đẩy các cơ quan sau phúc mạc: thận, tụy, đại tràng lên, đại tràng xuống, tá tràng và mạch máu. => Case lâm sàng 1: => Case lâm sàng 2: – Có thể khó đánh giá vị trí chính xác khối u trong trường hợp có kích thước lớn hoặc tổn thương mạc treo. * Dấu hiệu móng vuốt / Dấu hiệu mỏ (Claw sign / Beak sign) – Một khối u có nguồn gốc từ một cơ quan cụ thể sẽ tạo thành các góc tiếp xúc là góc nhọn với cơ quan đó và có ít nhất một phần bao quanh nó theo hình móng vuốt hoặc hình mỏ (Claw sign / Beak sign +) => Case lâm sàng 1: => Case lâm sàng 2: => Case lâm sàng 3: – Ngược lại, khối u bắt nguồn từ một cấu trúc liền kề sẽ đè đẩy cơ quan đó, không có phần của cơ quan đó bao quanh nó theo hình móng vuốt hoặc hình mỏ, góc tiếp xúc với cơ quan đó là góc tù (Claw sign / Beak sign -) => Case lâm sàng 1: khối u tuyến thượng thận => Case lâm sàng 2: khối u tuyến thượng thận => Case lâm sàng 3: khối u tuyến thượng thận => Case lâm sàng 4: khối u tuyến thượng thận * Embedded organ sign – Ngược lại, một khối u tiếp giáp nhưng không bắt nguồn từ cấu trúc tạng rỗng sẽ đè ép cấu trúc tạng rỗng đó biến dạng hình lưỡi liềm (Embedded organ sign -). * Invisible organ sign (Phantom organ sign) * Prominent Feeding Artery Sign – Morgagni năm 1761 đã mô tả một u mỡ sau phúc mạc trên tử thi. * U nguyên phát sau phúc mạc * Đặc điểm tổn thương => Sarcoma mỡ: – Tổn thương dạng nang – Liposarcoma là một khối u mô mỡ ác tính, có thể xảy ra ở bất kỳ vị trí nào trong cơ thể nhưng thường xuyên nhất ở các chi và sau phúc mạc. => Case lâm sàng 1: – Leiomyosarcoma là khối u ác tính của tế bào cơ trơn, với vị trí sau phúc mạc trong 12-69% trường hợp. Đây là loại sarcoma ác tính nguyên phát sau phúc mạc phổ biến thứ hai, chiếm 28% các trường hợp. – Các khối u xơ đơn độc, trước đây được gọi là u trung biểu mô khu trú hiếm gặp phát sinh từ các tế bào giống như nguyên bào sợi trong mô liên kết. Chúng thuộc cùng một loại khối u với u tế bào quanh mạch máu và hai thuật ngữ này thường được sử dụng thay thế cho nhau. – U sợi thần kinh là khối u vỏ thần kinh lành tính bao gồm các tế bào Schwann tân sinh lành tính xen kẽ với nguyên bào sợi, collagen và chất nền myxoid. – Schwannomas là một loại u vỏ thần kinh lành tính khác chiếm 4% trong tất cả các khối u sau phúc mạc. – U hạch thần kinh là khối u lành tính phát sinh từ hạch giao cảm cạnh cột sống và chiếm 0,7-1,6% trong tất cả các khối u nguyên phát sau phúc mạc. – U cận hạch, còn được gọi là u tế bào ưa crôm ngoài thượng thận, là khối u hiếm gặp có nguồn gốc tế bào chromaffin phát sinh từ các tế bào cận hạch ngoài thượng thận trong chuỗi giao cảm hoặc phó giao cảm. – U mạch bạch huyết (Lymphangioma) là một khối dạng nang lành tính bao gồm các kênh bạch huyết bị giãn, hình thành thứ phát sau sự thất bại trong việc thông hoặc dẫn lưu các kênh bạch huyết bình thường. Chúng được coi là một dạng dị dạng mạch máu dòng chảy chậm. => Case lâm sàng 1: – Xơ hóa sau phúc mạc là một phản ứng xơ hóa không phổ biến lần đầu tiên được bác sĩ tiết niệu người Pháp Albarran mô tả vào năm 1905 với tình trạng tắc nghẽn niệu quản thứ phát do xơ hóa ở khoang sau phúc mạc. => Case lâm sàng 1: => Case lâm sàng 2: => Case lâm sàng 3:I. Khoang sau phúc mạc
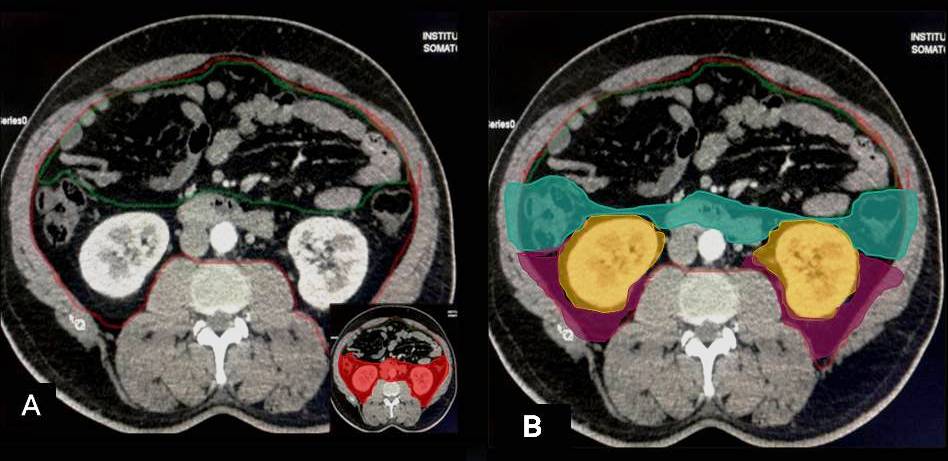
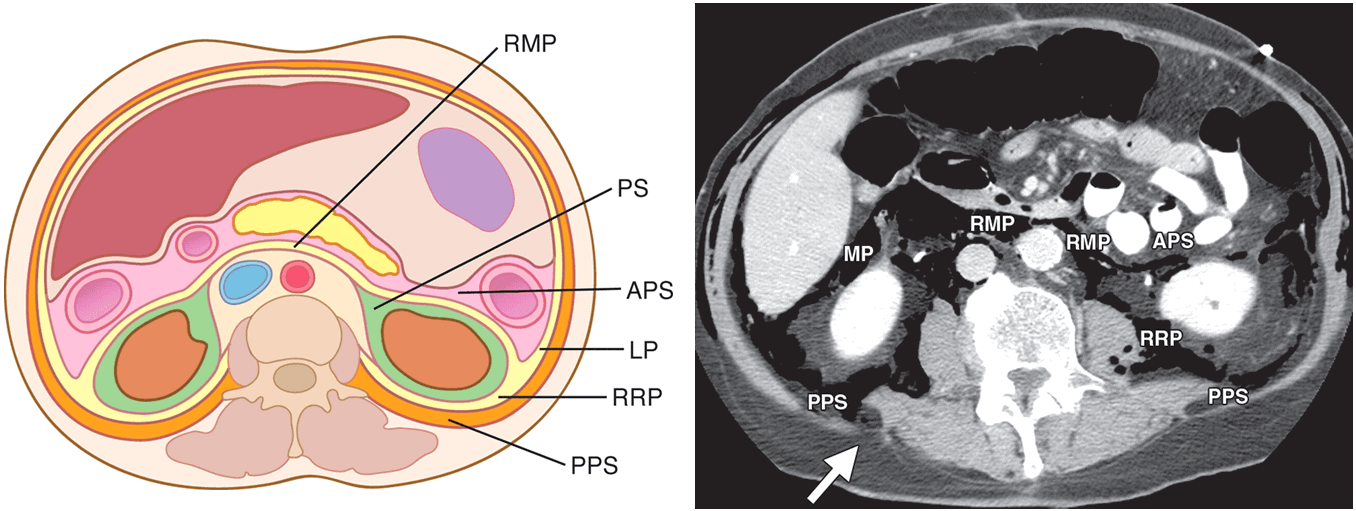
– Gồm 2 khoang bên và 1 khoang mạch máu trung tâm.
– Mỗi khoang bên gồm 3 khoang phân chia bởi mạc thận:
+ Khoang cạnh thận trước
+ Khoang cạnh thận sau
+ Khoang quanh thận.
– APS (Anterior pararenal space): khoang cạnh thận trước
– PPS: (Posterior pararenal space): khoang cạnh thận sau
– PS (Pararenal space): khoang quanh thận
– RMP (Retromesenteric plane): mặt phẳng sau mạc treo
– RRP (Retrorenal plane): mặt phẳng sau thận
– LCP (Lateralconal plane): mặt phẳng cạnh nón.1. Khoang cạnh thận trước
+ Phía trước: bởi phúc mạc thành.
+ Phía sau: mạc quanh thận
– Gồm các cấu trúc:
+ Tụy (đầu, thân, đuôi)
+ Đại tràng phải
+ Đại tràng trái
+ Tá tràng (khúc II, III)2. Khoang cạnh thận sau
+ Phía sau: mạc ngang
+ Phía trước và bên: mạc quanh thận
+ Nằm sau bên cơ vuông thắt lưng
– Thành phần: chứa 2 dải mỡ, mô liên kết, thần kinh.3. Khoang quanh thận
+ Phía trước: cân Gerota
+ Phía sau: cân Zuckerkandl
– Thần phần: thận và tuyến thượng thận, đoạn trên niệu quản, mạch thận, mạch quanh thận, mô mỡ.
– Có vách nối và mạng lưới bạch huyết phong phú cho phép sự lan tràn của bệnh lý từ các khoang lân cận.
– Hợp nhất của 2 cân ở dưới => thường không mở rộng xuống tiểu khung được.4. Khoang quanh mạch máu
– Thành phần: động mạch chủ bụng, tĩnh mạch chủ dưới, mỡ, hạch.
– Một vài bệnh lý hay gặp:
+ Xơ hóa khoang sau phúc mạc
+ Viêm quanh động mạch
+ Xuất huyết từ rò của phình động mạch chủ
+ Bệnh lý hạch5. Mạc quanh thận
+ Mạc thận trước (Mạc Gerota)
+ Mạc thận sau (Mạc Zuckerkandl)
+ Cân nón bên
+ Mạc ngang6. Mặt phẳng gian cân
+ Giữa khoang cạnh thận trước và khoang quanh thận
+ Vượt qua đường giữa
+ Con đường chính lan rộng dịch trong viêm tụy cấp
+ Thường nhầm với tụ dịch trong khoang cạnh thận trước.
+ Giữa khoang quanh thận và khoang sau thận
+ Không vượt qua đường giữa
+ Dịch trong khoang cạnh thận trước và mặt phẳng sau mạc treo có thể mở rộng vào mặt phẳng sau thận.7. Mặt phẳng gian cân
8. Cầu nối quanh thận
II. Khoang trước phúc mạc
– Ở phía sau, nó nằm sâu đến mạc ngang và lấp đầy khoang cạnh thận sau.
– Ở phía ngoài, nó dày lên và tạo thành đệm mỡ trước phúc mạc, là phần mỡ rộng phía trước của khoang cạnh thận sau.
– Phía dưới nó liên tục với phần mở rộng vùng chậu của khoang cạnh thận sau.III. U sau phúc mạc
1. Vị trí khối u
+ Khối u tiếp xúc với các cơ quan sau phúc mạc.2. Nguồn gốc khối u
– Một khối u phát sinh từ một cơ quan thường nằm bên trong cơ quan đó và ranh giới giữa khối u và cơ quan đó thường không rõ (Embedded organ sign +).
– Một khối lượng u kích thước lớn, đặc biệt là khi phát sinh từ một cơ quan kích thước nhỏ (tuyến thượng thận) có thể làm cho cấu trúc cơ quan đó bị phá hủy dẫn tới bị che lấp không thể xác định. Tuy nhiên có thể dương tính giả do cấu trúc cơ quan kích thước nhỏ bị đè ép dẫn tới khó đánh giá trên hình ảnh.
– Các khối u giàu mạch được cấp máu bởi nguồn động mạch nuôi được xác định rõ trên cắt lớp vi tính hoặc cộng hưởng từ => đặc điểm quan trọng gợi ý nguồn gốc khối u.3. Tiếp cận chẩn đoán
– Lobstein (1892) lần đầu tiên đã dùng danh từ “u sau phúc mạc”.
– U sau phúc mạc nguyên phát chiếm dưới 0,2% các loại ung thư và 60% trường hợp ở người trên 40 tuổi. Ở trẻ em trai, các u thuộc hệ giao cảm thường gặp trong khi các u quái hay gặp ở trẻ em gái.
– Phần lớn các trường hợp là khối u ác tính, trong đó khoảng 75% là khối u có nguồn gốc trung mô.
– Khi chúng không có nguồn gốc từ các cơ quan như thận, tuyến thượng thận, niệu quản, tuyến tụy hoặc các mạch máu lớn các khối sau phúc mạc được phân loại là nguyên phát.
– Tổn thương dạng khối đặc4. U sau phúc mạc
* Sarcoma mỡ
– Nó chiếm khoảng 15% của tất cả các khối u mô mềm, với 10-20% phát sinh ở sau phúc mạc.
– Là sarcoma nguyên phát sau phúc mạc phổ biến nhất, chiếm 35% tất cả các khối u mô mềm ác tính sau phúc mạc ở bệnh nhân trưởng thành.
– Lượng chất béo trong khối u thường tỷ lệ nghịch với cấp độ của khối u.
– Phân loại:
+ Khối u mỡ không điển hình, sarcoma mỡ biệt hoá tốt, sarcoma mỡ biệt hoá
+ Sarcoma mỡ dạng nhầy, sarcoma mỡ tế bào tròn
+ Sarcoma mỡ đa hình
– Đặc điểm hình ảnh:
+ U mỡ không điển hình, u mỡ biệt hoá tốt có xu hướng ưu tiên các chi, sau phúc mạc, vùng cận tinh hoàn và vùng bẹn. Hình ảnh chủ yếu là mô mỡ trên CT và MRI, nhưng cũng có thể nhìn thấy vách ngăn dày (> 2 mm), các thành phần mô mềm dạng nốt hoặc khối mô mềm < 1cm. Trong một số trường hợp, thành phần không phải mỡ chiếm ưu thế và có thể rất lớn.
+ Sarcoma mỡ biệt hóa tốt là những khối u độ ác tính thấp không di căn. Nguy cơ tái phát cao một phần là do khó cắt bỏ hoàn toàn do khối u thường không thể tách rời khỏi các cấu trúc lân cận. Sự biệt hóa có thể xảy ra ở những khối u này, thường phụ thuộc vào thời gian và phổ biến nhất ở LPS biệt hóa tốt của vùng sau phúc mạc, gặp tới 15% trường hợp. Sự hiện diện của sự biệt hóa được gợi ý trên hình ảnh bởi nốt mô mềm khu trú > 1cm, thường ở sau phúc mạc.
+ Các đặc điểm hình ảnh hướng tới chẩn đoán u mỡ biệt hóa tốt so với u mỡ lành tính bao gồm kích thước tổn thương ≥ 10 cm và sự hiện diện của nốt suy giảm mô mềm.
+ Di căn xa từ sarcoma mỡ biệt hóa xảy ra ở 15–20% trường hợp và vị trí phổ biến nhất là gan và phổi.
+ Sarcoma mỡ dạng nhầy và tế bào tròn thường xảy ra ở người trẻ tuổi. Các khối u có thành phần tế bào tròn lớn hơn (> 5%) sẽ tiến triển tích cực hơn với nguy cơ di căn và tử vong cao hơn. Các khối u thuộc loại này thường xuất hiện dưới dạng một khối ở các mô sâu của đùi và chỉ chứa một lượng nhỏ mỡ cực nhỏ (thường <10% thể tích khối u).
+ Sarcoma mỡ dạng nhầy có hình dạng đặc trưng trên MRI. Thường được xem là một khối đa thùy, hàm lượng nước cao trong các khối u này tạo ra cường độ tín hiệu thấp trên T1W và cường độ tín hiệu cao trên các chuỗi xung T2W. Vách ngăn mỡ (T1W-tăng tín hiệu) và tăng quang lan tỏa sau khi tiêm thuốc cản quang. Các vị trí di căn phổ biến nhất bao gồm vùng cạnh cột sống, xương, sau phúc mạc và chi đối diện.
+ Sarcoma mỡ đa hình là loại phụ ít phổ biến nhất, thường xảy ra nhất ở các mô mềm sâu ở tứ chi ở bệnh nhân cao tuổi. Tỷ lệ tái phát và di căn cao. Trên CT và MRI, hình ảnh là một khối mô mềm có giới hạn rõ chứa ít hoặc không có mỡ tương tự như các sarcoma mô mềm xâm lấn khác, thường biểu hiện xuất huyết nội và hoại tử.* Sarcoma cơ trơn
– Thường được chẩn đoán trong thập kỷ thứ năm đến thứ sáu của cuộc đời, thường gặp ở phụ nữ hơn nam giớ.
– Được cho là bắt nguồn từ các mạch máu lớn ở sau phúc mạc (tĩnh mạch chủ dưới) và/hoặc các nhánh của chúng. Tuy nhiên, ung thư cơ trơn biểu hiện phổ biến nhất dưới dạng khối u ngoài mạch máu (62% trường hợp) và hiếm khi hoàn toàn nằm trong mạch máu. Trong 33% trường hợp, ung thư cơ trơn có cả thành phần nội mạch và ngoại mạch. Tương tự như sarcoma mỡ, sarcom cơ trơn thường lớn khi bệnh nhân xuất hiện và các triệu chứng thường liên quan đến chèn ép các cấu trúc lân cận.
– Di căn được phát hiện tại thời điểm chẩn đoán ở 9% bệnh nhân có khối u ngoài mạch máu và 23% bệnh nhân có khối u trong mạch máu. Phổi, gan và phúc mạc là những vị trí phổ biến nhất.
– Đặc điểm hình ảnh:
+ Biểu hiện là khối mô mềm lớn, không đồng nhất bên trong và ngấm thuốc không đồng nhất do hoại tử và xuất huyết.
+ Kích thước khối u trung bình đối với các tổn thương có và không có sự tham gia của mạch máu đã được báo cáo lần lượt là 10,4cm và 11,3cm.
+ Vôi hóa và mỡ hiếm gặp.
+ Các tổn thương nội mạch đơn thuần xuất hiện dưới dạng các khối giãn nở ngấm thuốc không đồng nhất.
+ Chúng thường thể hiện tín hiệu từ thấp đến trung bình trên T1W và cường độ tín hiệu từ trung bình đến cao trên T2W. Đôi khi chúng cũng biểu hiện mức dịch thứ phát sau xuất huyết.* U xơ đơn độc
– Khoảng 1/3 các khối u xơ đơn độc nằm trong ổ bụng và vị trí phổ biến nhất là sau phúc mạc.
– Phần lớn bệnh nhân được chẩn đoán trong thập kỷ thứ năm đến thứ bảy của cuộc đời, nhưng khối u có thể phát sinh ở mọi lứa tuổi.
– Hầu hết các khối u xơ đơn độc đều lành tính, với tỷ lệ ác tính ước tính là 20%–40%.
– Các khối u xơ đơn độc sau phúc mạc thường không có triệu chứng ban đầu và có thể phát triển lớn trước khi gây ra các triệu chứng.
– Tỷ lệ nhỏ các khối u xơ đơn độc sau phúc mạc có liên quan đến hội chứng cận ung thư, phổ biến nhất là hội chứng Doege-Potter, xảy ra ở những bệnh nhân bị hạ đường huyết thứ phát do sản xuất quá mức yếu tố tăng trưởng giống insulin 2 từ các tế bào khối u.
– Đặc điểm hình ảnh:
+ Tỷ trọng không đồng nhất và có nhiều mạch máu, với các mạch máu phụ nổi rõ.
+ Hiếm khi có biểu hiện thoái hóa dạng nang, hoại tử và vôi hóa.
+ Cường độ tín hiệu có thể thay đổi và phụ thuộc vào tế bào và sự phong phú của chất nền myxoid và/hoặc mô xơ. Thường giảm tín hiệu đến đồng tín hiệu so với cơ trên T1W và giảm tín hiệu trên T2W.
+ Ngấm thuốc sau tiêm thường được ghi nhận và các khoảng trống dòng chảy (biểu hiện như các điểm giảm tín hiệu trên T1W và T2W) có thể xuất hiện do các mạch máu trong tổn thương nổi rõ.* U sợi thần kinh
– Chúng thường không được bao bọc và xen kẽ với các sợi thần kinh. U sợi thần kinh có thể xảy ra ở da hoặc mô mềm sâu và chúng chiếm 1% trong tất cả các khối u sau phúc mạc.
– Các u sợi thần kinh khu trú đơn độc thường lẻ tẻ và không liên quan đến u xơ thần kinh loại 1, trong khi nhiều u sợi thần kinh dạng đám rối gần như luôn liên quan đến u xơ thần kinh loại 1.
– Tuổi khởi phát ở bệnh nhân u sợi thần kinh đơn độc là 20–30 tuổi, nhưng u xơ thần kinh ở bệnh nhân u xơ thần kinh loại 1 thường xuất hiện ở độ tuổi sớm hơn.
– U xơ thần kinh thường được phát hiện tình cờ khi chúng phát sinh ở sau phúc mạc vì chúng thường không có triệu chứng.
– Đặc điểm hình ảnh:
+ U sợi thần kinh khu trú thường biểu hiện rõ như khối giảm đậm độ tối thiểu được xác định rõ (20–40 HU) trên CT.
+ Chúng thường cho tín hiệu đồng tín hiệu đến giảm cường độ so với cơ ở T1W và tăng cường độ tín hiệu ở MRI nhạy cảm với chất lỏng, với sự tăng cường thay đổi.
+ Dấu hiệu bia bắn: bao gồm một tiêu điểm trung tâm có cường độ tín hiệu thấp của mô sợi collagen dày đặc ở trung tâm, bao quanh tăng tín hiệu của myxoid ngoại vi ở T2W.
+ U sợi thần kinh dạng đám rối có xu hướng biểu hiện dưới dạng các khối thâm nhiễm lớn có nhiều thùy hoặc một tập hợp các khối dọc theo các sợi thần kinh. U sợi thần kinh đám rối sau phúc mạc có xu hướng ở hai bên, đối xứng và song song với cơ thắt lưng, đây có thể là một đầu mối hình ảnh quan trọng để phân biệt chúng với các sarcoma sau phúc mạc khác.* U bao sợi thần kinh
– Trái ngược với u xơ thần kinh, chúng chỉ được tạo thành từ các tế bào Schwann tân sinh lành tính và có thể tách rời khỏi các sợi thần kinh. Do đó, chúng có xu hướng phát triển lệch tâm từ các sợi thần kinh ngoại vi.
– Schwannomas có thể xảy ra ở mọi lứa tuổi nhưng phổ biến hơn giữa thập kỷ thứ hai và thứ năm của cuộc đời.
– Hầu hết các trường hợp là lẻ tẻ, ngoại trừ một phần nhỏ các trường hợp có thể liên quan đến u xơ thần kinh loại 2.
– Thoái hóa ác tính hiếm gặp ở u bao sợi thần kinh. Chúng cũng ít có khả năng tạo ra các triệu chứng hơn so với u xơ thần kinh và tỷ lệ phẫu thuật cắt bỏ thành công thường cao hơn.
– Đặc điểm hình ảnh:
+ U bao sợi thần kinh thường không thể phân biệt được với u xơ thần kinh trên hình ảnh.
+ Chúng thường xuất hiện dưới dạng các khối giảm tỷ trọng hình thoi hoặc hình thoi.
+ Đặc điểm cường độ tín hiệu điển hình của u bao sợi thần kinh trên MRI cũng tương tự như đặc điểm của u xơ thần kinh, với cường độ tín hiệu trung bình ở MRI có trọng số T1W (tương đương với giảm tín hiệu đối với cơ) và cường độ tín hiệu cao ở MRI có trọng số T2W.
+ Tăng cường thay đổi được nhìn thấy trên CT và MRI.
+ Có thể biểu hiện dấu hiệu bia bắn, mặc dù nó ít gặp hơn so với u xơ thần kinh.
+ Thoái hóa dạng nang thường thấy ở u bao sợi thần kinh sau phúc mạc khi chúng phát triển lớn hơn 5 cm.
+ U bao sợi thần kinh có thể biểu hiện vôi hóa và xuất huyết.* U hạch thần kinh
– Bên trong, những khối u này bao gồm các tế bào mào thần kinh nguyên thủy trưởng thành.
– Chúng thường không có triệu chứng và biểu hiện ở trẻ em, thanh thiếu niên và thanh niên, chủ yếu là nữ giới.
+ U hạch thần kinh có thể phát sinh từ u nguyên bào thần kinh trưởng thành hoặc u nguyên bào thần kinh hạch.
– Chúng hiếm khi tiết đủ lượng catecholamine để gây ra các triệu chứng giao cảm như đỏ bừng mặt.
– Phẫu thuật cắt bỏ hoàn toàn có thể chữa khỏi bệnh ở hầu hết bệnh nhân.
– Đặc điểm hình ảnh:
+ U hạch thần kinh biểu hiện điển hình như một khối cạnh cột sống định hướng theo chiều dọc ở sau phúc mạc hoặc trung thất sau. Ở sau phúc mạc, u hạch có thể phát sinh từ chuỗi giao cảm (phổ biến hơn) hoặc từ tủy thượng thận.
+ Trên CT, chúng biểu hiện dưới dạng một khối đồng nhất giảm đậm độ nhẹ được xác định rõ với ngấm thuốc thay đổi.
+ Có thể thấy vôi hóa trong 25% trường hợp và thường có dạng chấm hoặc lốm đốm, trong khi hoại tử trung tâm và xuất huyết hiếm khi gặp.
+ Cường độ tín hiệu không đồng nhất trên T1W và T2W, với mức độ tăng tín hiệu trên T2W tương quan thuận với cường độ tín hiệu của chất nền myxoid được tìm thấy tại chỗ. Hình dạng cuộn tròn cũng đã được mô tả trên MRI T2W và biểu hiện dưới dạng các dải đường cong bên trong có cường độ tín hiệu thấp. Chúng được cho là đại diện cho các vùng xen kẽ của tế bào Schwann và sợi collagen trong chất nền myxoid nền biểu thị cường độ tín hiệu cao xung quanh trong tổn thương trên T2W.
+ Gado: thiếu sự tăng cường sớm, với sự gia tăng dần dần trong các giai đoạn chậm hơn. Điều này được cho là xảy ra do chất nền myxoid dồi dào, có thể dẫn đến chậm tích lũy dần dần chất cản quang trong khoang ngoại bào.* U cận hạch
– U cận hạch giao cảm tiết ra catecholamine và khoảng 40% bệnh nhân mắc chúng có biểu hiện lâm sàng liên quan đến dư thừa catecholamine, bao gồm tăng huyết áp và nhịp tim nhanh.
– U cận hạch giao cảm nằm ở đáy sọ và cổ và có liên quan đến các nhánh của dây thần kinh thiệt hầu và dây thần kinh phế vị, trong khi u cận hạch giao cảm phát sinh ở bất cứ đâu dọc theo chuỗi giao cảm, phổ biến nhất là ở bụng (khoảng 75% của tất cả các u cận hạch giao cảm). Do đó, u cận hạch sau phúc mạc hầu như chỉ là u cận hạch giao cảm.
– Trong ổ bụng, vị trí phổ biến nhất của u cận hạch nguyên phát là cơ quan Zuckerkandl, nằm ở nguồn gốc của động mạch mạc treo tràng dưới gần chỗ chia đôi động mạch chủ.
– U cận hạch có liên quan đến một số rối loạn di truyền trong khoảng 30%–40% trường hợp, bao gồm hội chứng đa tân sinh nội tiết và hội chứng von Hippel–Lindau.
– Độ tuổi trung bình khi xuất hiện bệnh nhân mắc u cận hạch là trong thập kỷ thứ hai đến thứ tư của cuộc đời. Chẩn đoán có thể được thực hiện trên lâm sàng trên cơ sở phát hiện nồng độ axit metanephrine hoặc vanillylmandelic tăng cao trong nước tiểu.
– Nguy cơ ác tính ở các u cận hạch giao cảm được ước tính trong khoảng 30%–40%.
– Điều trị thường bao gồm phẫu thuật cắt bỏ và xạ trị sau phẫu thuật. Điều trị nội khoa trước phẫu thuật bằng thuốc chẹn α-adrenergic là rất quan trọng để ngăn ngừa các biến chứng đe dọa tính mạng thứ phát do giải phóng catecholamine trong phẫu thuật.
– Đặc điểm hình ảnh:
+ U cận hạch lành tính và ác tính rất khó phân biệt trên cơ sở hình ảnh học trừ khi khối u xuất hiện xâm lấn tại chỗ hoặc có di căn tại thời điểm chẩn đoán.
+ Trên CT, u cận hạch thường không đồng nhất và thường có thể nhìn thấy hoại tử, xuất huyết và/hoặc vôi hóa.
+ Tăng cường chất cản quang thường được ghi nhận do tăng sinh mạch máu, đặc biệt là ngoại vi.
+ T2W: cường độ tín hiệu cao khuếch tán (dạng “bóng đèn”) thường được mô tả trong u cận hạch. Tuy nhiên, biểu hiện phức tạp hơn thường được quan sát thấy do tín hiệu không đồng nhất có liên quan đến xuất huyết và/hoặc hoại tử.
+ T1W: thường cho thấy cường độ tín hiệu từ trung bình đến thấp. Các vùng tăng tín hiệu trên T1W có thể là thứ phát sau xuất huyết).
+ Các khoảng trống cường độ tín hiệu trên T1W và T2W có thể tạo ra hình dạng “muối và tiêu” điển hình.* U mạch bạch huyết
– Có thể xuất hiện ở mọi lứa tuổi nhưng thường gặp nhất ở trẻ em (~90% ở trẻ < 2 tuổi).
– Phần lớn (95%) xuất hiện ở vùng cổ và nách; khoảng 5% ở mạc treo, sau phúc mạc, phúc mạc tạng ổ bụng, phổi và trung thất (5%).
– U mạch bạch huyết ổ bụng thường gặp ở mạc treo, mạc nối, cạnh đại tràng và sau phúc mạc. U mạch bạch huyết mạc treo có thể gây biến chứng như tắc ruột non hoặc xoắn ruột, nhồi máu mạc treo.
– U mạch bạch huyết sau phúc mạc có khuynh hướng phát triển kéo dài ra do các khoang giải phẫu thường có vách ngăn theo chiều ngang.
– U mạch bạch huyết sau phúc mạc:
+ Dị dạng bạch huyết sau phúc mạc chiếm khoảng 1% trong tổng số các trường hợp dị dạng bạch huyết, 5% tổng số các trường hợp trong ổ bụng.
+ Thường xuất hiện nhiều hơn ở mạc treo, sau đó là mạc nối lớn, mạc treo đại tràng và sau đó là sau phúc mạc.
+ Thường không có triệu chứng và được phát hiện tình cờ qua hình ảnh học. Hiếm khi, chúng có thể xuất hiện dưới dạng một khối u có thể sờ thấy được.
+ Biểu hiện khối u nang đa buồng rõ ràng với dịch trong nang đồng nhất.
+ Vôi hóa hiêm gặp.
+ Sau tiêm có thể ngấm thuốc thành và vách nang.
+ Chúng có thể vượt qua các mặt phẳng cân cơ và liên quan đến nhiều khoang khác nhau. Thường là các tổn thương lớn, kéo dài qua các khoang giải phẫu lân cận.
* Xơ hóa sau phúc mạc
– Tình trạng này trước đây đã được mô tả là viêm quanh động mạch chủ mạn tính, viêm quanh niệu quản và u hạt sau phúc mạc xơ cứng.
– Bệnh thường gặp ở những người từ 40–60 tuổi và nam giới có khả năng mắc xơ hóa phúc mạc cao gấp hai đến ba lần so với phụ nữ.
– Hầu hết (> 70%) trường hợp được cho là vô căn (bệnh Ormond); số còn lại xảy ra liên quan đến các rối loạn viêm (viêm tụy, viêm bể thận), tia xạ hoặc thuốc, tiếp xúc amiang, chảy máu sau phúc mạc.
– Bệnh này là một phần của một loạt các thực thể có quá trình gây bệnh chung bao gồm phản ứng viêm với tình trạng xơ vữa động mạch chủ bụng tiến triển, kết hợp với các yếu tố tự miễn:
+ Xơ hóa sau phúc mạc vô căn
+ Xơ hóa sau phúc mạc quanh phình động mạch
+ Viêm quanh động mạch chủ đơn độc
+ Viêm phình động mạch chủ
– Đặc điểm hình ảnh:
+ Xơ hóa sau phúc mạc thường biểu hiện dưới dạng khối mô mềm sau phúc mạc, không đồng nhất, ranh giới rõ nhưng nằm trước cột sống, có mật độ bằng cơ xung quanh.
+ Ban đầu có xu hướng bắt đầu gần mức phân chia động mạch chủ chậu, mô bất thường này phân nhánh để đi theo động mạch chậu chung và lan lên trên có thể bao phủ rốn thận. Có thể xảy ra sự mở rộng đáng kể về phía trước liên quan đến tá tràng, tụy và lách. Nó bao phủ nhưng không xâm lấn hoặc hẹp niệu quản hoặc mạch máu, không đè đẩy mạch máu. Tuy nhiên, tắc nghẽn niệu quản và huyết khối tĩnh mạch có thể xảy ra.
+ Mức độ ngấm thuốc tương quan với hoạt động của quá trình xơ hóa. Ngấm thuốc có thể thấy trong giai đoạn cấp tính, với mức tăng 20–60HU. Có thể thấy ngấm thuốc ít hoặc không ngấm thuốc trong giai đoạn không hoạt động hoặc mãn tính.
Tài liệu tham khảo
* Peritoneal and Retroperitoneal Anatomy and Its Relevance for Cross-Sectional Imaging – Temel Tirkes , Kumaresan Sandrasegaran, Aashish A. Patel
* An easy way to understand the retroperitoneal anatomy and their most frequent pathology – M. Camargo Montanari, M. Rascón Risco, F. Cabrera Canal
* Anatomy of the retroperitoneal space – N. Achour, M. M. Kalai, A. Ben Miled
* Aorto-Caval Space: a forgotten retroperitoneal space – F. G. D. L. Leiter Herran, P. Sepulveda, A. Rojas Astorga
* The spaces of the retroperitoneum: A pictorial review – A. Almeida, M. Castro, J. Loureiro
* Radioanatomy of the retroperitoneal space – A.CoffinI.Boulay-ColettaD.Sebbag-SfezM.Zins
* Extraperitoneal Space: Anatomic and Radiologic Overview – M. Horta, N. Neto, C. Couceiro, L. P. Martins; Lisbon/PT
* Unraveling the retroperitoneum – D. Roriz, I. Abreu, P. Belo-Soares
* Primary retroperitoneal tumors, Can we narrow the differential diagnosis? – A. H. A. Mohamed, H. Wahba, S. A. A. Z. Hanna; Cairo/EG
* Practical approach to primary retroperitoneal masses in adults – Micaela Maciel dos Santos Mota
* Solid malignant retroperitoneal masses – a pictorial review – Cressida Brennan, Dilkash Kajal, Korosh Khalili
* Primary Retroperitoneal Neoplasms: CT and MR Imaging Findings with Anatomic and Pathologic Diagnostic Clues – Mizuki Nishino, Katsumi Hayakawa, Manabu Minami
* Imaging of Uncommon Retroperitoneal Masses – Prabhakar Rajiah , Rakesh Sinha, Carlos Cuevas
* Fat-containing Retroperitoneal Lesions: Imaging Characteristics, Localization, and Differential Diagnosis – Akram M. Shaaban , Maryam Rezvani, Marc Tubay
* MDCT signs differentiating retroperitoneal and intraperitoneal lesions- diagnostic pearls – D. V. Bhargavi, R. Avantsa, P. Kala; Bangalore/IN
* Radiologic-Pathologic Correlation of Primary Retroperitoneal Neoplasms – Khalid Al-Dasuqi, Lina Irshaid, Mahan Mathur
* Imaging of Liposarcoma: Classification, Patterns of Tumor Recurrence, and Response to Treatment – Kevin N. O’Regan, Jyothi Jagannathan, Katherine Krajewski
* Retroperitoneal Fibrosis: A Review of Clinical Features and Imaging Findings – Carmel G. Cronin, Derek G. Lohan, Michael A. Blake






# Cập nhật nội dung bài viết & Case lâm sàng 10/6/2023
# Cập nhật nội dung bài viết & Case lâm sàng 30/5/2023
# Cập nhật nội dung bài viết & Case lâm sàng 12/8/2023
# Cập nhật nội dung bài viết & Case lâm sàng 30/1/2023
# Cập nhật nội dung bài viết & Case lâm sàng 25/11/2022